Вода является наилучшим растворителем: в ней в той или иной степени растворяются почти все неорганические вещества и немало органических.
В морях и океанах находятся в растворенном состоянии свыше 60 элементов периодической системы. Так, золота в Мировом океане содержится столько, что если его полностью извлечь, то на каждого жителя Земли достанется по 3 килограмма. Казалось бы, много. В предыдущем разделе мы указывали, сколько воды содержит мировой океан. Если поделить все золото на объем воды в океане, то получим концентрацию 0,01 мг/м3 воды. При такой концентрации и нынешнем уровне техники добывать золото из океана нерационально. Для сравнения приведем другую цифру: уран добывают при концентрации свыше 2 мг/м3 раствора.
Водопровод в Древнем Риме был выложен изнутри свинцом. Протяженность водопровода составляла 443 км. Расход воды, как мы уже указывали,— до 3 л на каждого жителя ежедневно. В этой воде, конечно, понемногу растворялся свинец, и жители Вечного Города получали с пищей избыточное количество этого тяжелого и ядовитого металла. Как показали археологические раскопки, кости древних римлян, действительно, имеют повышенное содержание свинца. Возможно, отравление свинцом было причиной смерти многих жителей Древнего Рима.
Вода легко поглощает газы, в том числе и такие, которые при соединении с водой образуют кислоты, а кислая вода обладает повышенной растворяющей способностью. В кислотах, например, растворяются (правильнее сказать: с кислотами взаимодействуют) металлы.
На некоторых металлургических и химических предприятиях, где плохо ведется газоочистка, из труб идет цветной дым. Дым рыжего цвета в обиходе называют «лисьим хвостом» — это газ NO2 (вместе с несгорев — шими частицами). Соединяясь с парами воды, оксид азота(IV) образует в атмосфере смесь кислот:
2N02 + H20 = HN03 + HN02.
Потом с росой или дождем азотная HNO3 и азотистая HNO2 кислоты попадают на землю, вызывая повышенную коррозию металлических изделий.
В газовых выбросах ряда предприятий содержится оксид серы(IV), который с парами воды образует сернистую кислоту:
S02 + H20 = H2S03.
Выпадающий в городе дождь содержит некоторое количество сернистой кислоты, а также серной, образующейся из оксида серы(VI). Дождь может быть и радиоактивным, если облако встретит на своем пути радиоактивные газовые выбросы. Наконец, дождевая вода содержит и растворенные соли в количестве до З мг на 1 дм3 воды. Таким образом, дождь и снег не могут быть примером чистого вещества.
В чистой воде водородный показатель рН должен быть равен 7,0. Именно таким мы вправе его ожидать в дистиллированной воде. Однако в действительности вода реагирует с СОо, содержащимся в воздухе:
С02 + Н20 = Н2С03.
Наличие угольной кислоты Н2СО3 обусловливает слабокислую реакцию дистиллированной воды: рН = = 6,54-6,0.
|
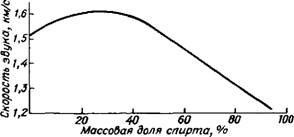
Рис. I. Изменение скорости звука в водных растворах этилового спирта с повышением концентрации |
Но если вода хотя бы частично растворяет стенки сосуда, в котором она находится, то даже дистиллированная вода может считаться чистой лишь в самом первом приближении. Гораздо чище дважды дистиллированная вода (бидистиллят), еще чище — трижды дистиллированная (тридистиллят). В 1894 г. Ф. Коль — рауш получил воду, которая до настоящего времени является рекордно чистой: он проводил дистилляцию 42 раза подряд, причем держал воду в сосуде, с которым работал до этого в течение 10 лет и из которого, таким образом, перешло в воду максимум возможного. Степень чистоты определяют по электрической проводимости; вода, полученная Кольраушем, имела проводимость в 100 раз меньше, чем обычная дистиллированная.
Вода, в которой растворено какое-то вещество, естественно, отличается по своим свойствам от чистой воды. Известно, например, что этиловый спирт хорошо растворяется в воде. При этом некоторые свойства воды изменяются незначительно: она остается прозрачной, маловязкой жидкостью. Зато изменяются запах, вкус, плотность, температура затвердевания и многие другие свойства. На рис. 1 показано, как изменяется такая характеристика, как скорость звука и. По мере добавления спирта к воде величина а — начиная с 20 % спирта — линейно уменьшается. Это кажется вполне естественным, так как для воды « = 1485 м/с, для спирта «=1173 м/с.
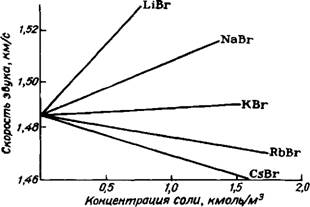
Если же добавлять к воде поваренную соль (хлорид натрия), то величина и начнет возрастать, и это
|
Рис. 2. Изменение скорости звука в водных растворах бромидов щелочных металлов с повышением концентрации |
Тоже кажется вполне естественным, ибо для монокристалла соли « = 4500 м/с. Однако, если сравнить разные соли, например группу бромидов щелочных металлов (рис. 2), то обнаружим странное явление: добавление некоторых солей вызывает понижение скорости звука. В монокристаллах таких солей (их известно более двух десятков) скорость звука выше, чем в воде, но меньше, чем во льду (для льда ы = 3800 м/с). Во всех остальных случаях скорость звука в кристаллах растворенных солей больше, чем во льду. Поэтому мы должны сделать вывод, что при растворении солей в воде существенное значение имеет лед, который, следовательно, присутствует в виде обособленной фазы.